Ăn mòn kim loại là gì?

Ăn mòn kim loại hàng năm tiêu tốn nhiều chi phí, thậm chí còn gây nguy hiểm cho các cấu kiện của các  nhà máy và chủ đầu tư các công trình dân dụng, công nghiệp, nông nghiệp, viễn thông, điện lực, dầu khí, quân sự, quốc phòng và đặc biệt là các công trình ven biển.
Theo như thống kê khối lượng kim loại bị ăn mòn trung bình hằng năm trên thế giới khoảng 10−30% khối lượng kim loại được sản xuất ra. Sự ăn mòn kim loại gây tổn thất lớn về nhiều mặt cho nền kinh tế và đời sống con người. Tuy nhiên, nếu hiểu rõ nguyên nhân gốc của vấn đề ăn mòn, chúng ta hoàn toàn có thể ngăn chặn và đẩy lùi ăn mòn.
Bước đầu tiên để kiểm soát các chi phí này là phải hiểu rõ ăn mòn là gì và nguyên nhân dẫn đến ăn mòn.
nhà máy và chủ đầu tư các công trình dân dụng, công nghiệp, nông nghiệp, viễn thông, điện lực, dầu khí, quân sự, quốc phòng và đặc biệt là các công trình ven biển.
Theo như thống kê khối lượng kim loại bị ăn mòn trung bình hằng năm trên thế giới khoảng 10−30% khối lượng kim loại được sản xuất ra. Sự ăn mòn kim loại gây tổn thất lớn về nhiều mặt cho nền kinh tế và đời sống con người. Tuy nhiên, nếu hiểu rõ nguyên nhân gốc của vấn đề ăn mòn, chúng ta hoàn toàn có thể ngăn chặn và đẩy lùi ăn mòn.
Bước đầu tiên để kiểm soát các chi phí này là phải hiểu rõ ăn mòn là gì và nguyên nhân dẫn đến ăn mòn.

 Như vậy về bản chất thì ăn mòn hóa học là quá trình oxi hóa – khử; trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường, ăn mòn xảy ra chậm. Còn ăn mòn điện hóa là sự ăn mòn kim loại do tác dụng của dung dịch chất điện li và tạo nên dòng điện. Ăn mòn điện hóa là ăn mòn kim loại phổ biến và nghiêm trọng nhất trong tự nhiên. Nó diễn ra nhanh hơn rất nhiều so với ăn mòn hóa học thông thường do có phát sinh dòng điện.
Như vậy về bản chất thì ăn mòn hóa học là quá trình oxi hóa – khử; trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường, ăn mòn xảy ra chậm. Còn ăn mòn điện hóa là sự ăn mòn kim loại do tác dụng của dung dịch chất điện li và tạo nên dòng điện. Ăn mòn điện hóa là ăn mòn kim loại phổ biến và nghiêm trọng nhất trong tự nhiên. Nó diễn ra nhanh hơn rất nhiều so với ăn mòn hóa học thông thường do có phát sinh dòng điện.
 đến trên 15 năm mà không cần bảo trì; dễ dàng thi công ngay cả với các cấu kiện có hình dạng phức tạp như van, khớp bích, bu lông, khủy ống vv.
đến trên 15 năm mà không cần bảo trì; dễ dàng thi công ngay cả với các cấu kiện có hình dạng phức tạp như van, khớp bích, bu lông, khủy ống vv.
 nhà máy và chủ đầu tư các công trình dân dụng, công nghiệp, nông nghiệp, viễn thông, điện lực, dầu khí, quân sự, quốc phòng và đặc biệt là các công trình ven biển.
Theo như thống kê khối lượng kim loại bị ăn mòn trung bình hằng năm trên thế giới khoảng 10−30% khối lượng kim loại được sản xuất ra. Sự ăn mòn kim loại gây tổn thất lớn về nhiều mặt cho nền kinh tế và đời sống con người. Tuy nhiên, nếu hiểu rõ nguyên nhân gốc của vấn đề ăn mòn, chúng ta hoàn toàn có thể ngăn chặn và đẩy lùi ăn mòn.
Bước đầu tiên để kiểm soát các chi phí này là phải hiểu rõ ăn mòn là gì và nguyên nhân dẫn đến ăn mòn.
nhà máy và chủ đầu tư các công trình dân dụng, công nghiệp, nông nghiệp, viễn thông, điện lực, dầu khí, quân sự, quốc phòng và đặc biệt là các công trình ven biển.
Theo như thống kê khối lượng kim loại bị ăn mòn trung bình hằng năm trên thế giới khoảng 10−30% khối lượng kim loại được sản xuất ra. Sự ăn mòn kim loại gây tổn thất lớn về nhiều mặt cho nền kinh tế và đời sống con người. Tuy nhiên, nếu hiểu rõ nguyên nhân gốc của vấn đề ăn mòn, chúng ta hoàn toàn có thể ngăn chặn và đẩy lùi ăn mòn.
Bước đầu tiên để kiểm soát các chi phí này là phải hiểu rõ ăn mòn là gì và nguyên nhân dẫn đến ăn mòn.
Ăn mòn là gì?
Ăn mòn kim loại là sự phá hủy kim loại hoặc hợp kim do tác động của môi trường như axit, muối, hóa chất vv. Hậu quả là kim loại bị oxi hóa thành các ion dương do các quá trình hóa học hoặc điện hóa.Các dạng ăn mòn:
Căn cứ vào môi trường và cơ chế của sự ăn mòn kim loại, người ta phân thành hai dạng chính: ăn mòn hóa học và ăn mòn điện hóa.Ăn mòn hóa học là quá trình oxi hóa – khử, trong đó kim loại phản ứng trực tiếp với các chất oxi hóa trong môi trường (các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường) và không có xuất hiện dòng điện
Thí dụ:
Ăn mòn điện hóa học là quá trình oxi hóa – khử; trong đó kim loại bị ăn mòn do tác dụng của dung dịch chất điện li và tạo nên dòng electron chuyển dời từ cực âm sang cực dương.
Điều kiện xảy ra ăn mòn điện hóa học: đồng thời cả 3 điều kiện sau:
- Các điện cực phải khác nhau về bản chất. Có thể là cặp hai kim loại khác nhau, kim loại – phi kim hay kim loại – hợp chất. Kim loại có thế điện cực chuẩn nhỏ hơn là cực âm
- Các điện cực phải tiếp xúc trực tiếp hoặc gián tiếp với nhau qua dây dẫn
- Các điện cực cùng tiếp xúc với dung dịch chất điện li
Ăn mòn điện hóa học hợp kim của sắt (gang, thép) trong không khí ẩm
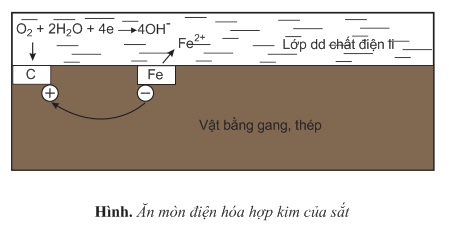
Gang, thép là hợp kim Fe – C gồm những tinh thể Fe tiếp xúc trực tiếp với tinh thể C đóng vai trò là 2 cực. Không khí ẩm có chứa H2O, CO2, O2…tạo ra lớp dung dịch chất điện li phủ lên bề mặt gang; thép làm xuất hiện vô số pin điện hóa mà Fe là cực âm, C là cực dương. Ở cực âm xảy ra sự oxi hóa: Fe → Fe2+ + 2e Ở cực dương xảy ra sự khử: 2H+ + 2e → H2 và O2 + 2H2O + 4e → 4OH– Tiếp theo: Fe2+ + 2OH– → Fe(OH)2 4Fe(OH)2 + O2(kk) + 2H2O → 4Fe(OH)3 – Theo thời gian Fe(OH)3 sẽ bị mất nước tạo ra gỉ sắt có thành phần chủ yếu là Fe2O3.xH2O Như vậy về bản chất thì ăn mòn hóa học là quá trình oxi hóa – khử; trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường, ăn mòn xảy ra chậm. Còn ăn mòn điện hóa là sự ăn mòn kim loại do tác dụng của dung dịch chất điện li và tạo nên dòng điện. Ăn mòn điện hóa là ăn mòn kim loại phổ biến và nghiêm trọng nhất trong tự nhiên. Nó diễn ra nhanh hơn rất nhiều so với ăn mòn hóa học thông thường do có phát sinh dòng điện.
Như vậy về bản chất thì ăn mòn hóa học là quá trình oxi hóa – khử; trong đó các electron của kim loại được chuyển trực tiếp đến các chất trong môi trường, ăn mòn xảy ra chậm. Còn ăn mòn điện hóa là sự ăn mòn kim loại do tác dụng của dung dịch chất điện li và tạo nên dòng điện. Ăn mòn điện hóa là ăn mòn kim loại phổ biến và nghiêm trọng nhất trong tự nhiên. Nó diễn ra nhanh hơn rất nhiều so với ăn mòn hóa học thông thường do có phát sinh dòng điện.
Giải pháp ngăn chặn ăn mòn được tìm ra
Sau nhiều năm nghiên cứu và thử nghiệm, các kỹ sư của tập đoàn Nitto Denko-Nhật Bản đã cho ra đời bộ sản phẩm chống ăn mòn NitoHullmac XG. Đây là bộ sản phẩm lý tưởng cho vấn đề ăn mòn, bảo vệ kết cấu thép từ trong ra ngoài với độ bền lên đến trên 15 năm mà không cần bảo trì; dễ dàng thi công ngay cả với các cấu kiện có hình dạng phức tạp như van, khớp bích, bu lông, khủy ống vv.
đến trên 15 năm mà không cần bảo trì; dễ dàng thi công ngay cả với các cấu kiện có hình dạng phức tạp như van, khớp bích, bu lông, khủy ống vv.
Cấu tạo bộ sản phẩm gồm 3 đến 4 lớp.
- Lớp sơn lót có tác dụng hấp thụ và trung hòa các tác nhân gây ăn mòn trên bề mặt kết cấu thép
- Lớp băng keo có tác dụng kép chống ăn mòn từ bên ngoài
- Lớp sơn phủ có tác dụng chống tia UV và chống thấm, ngăn ngừa các tác nhân gây ăn mòn sâm nhập vào bề mặt cấu kiện như bụi hóa chất; dung dịch, hơi nước muối biển gây ăn mòn.
- Tùy vào hình dạng phức tạp của cấu kiện; có thể cần sử dụng thêm sét trám khe để tạo phẳng và tạo thuận tiện cho việc cuốn băng keo tại các vị trí như mặt bích, van, khớp nối vv.


























